Les 6 raisons de choisir les vaccins Virbac

1. Virbac : un laboratoire pharmaceutique français
![raison-1-virbac-fr.png]()
-
Virbac est un laboratoire pharmaceutique français, implanté à Carros (06) depuis 1968. Aujourd'hui, nous sommes le 6ème laboratoire vétérinaire au monde. En tant que laboratoire familial indépendant, nous sommes 100 % dédiés à la santé animale.
- En France, 1 300 collaborateurs contribuent au tissu économique national et local.
- 80 % de nos produits sont fabriqués en France.
- Nous comptons 6 400 collaborateurs dans le monde.
L'excellence industrielle avec le projet Bio 5
Virbac a engagé un plan de transformation ambitieux pour faire de son site de Carros un Centre Mondial d'Excellence pour la fabrication de produits biologiques, dont les vaccins sont la pierre angulaire. Cela se concrétise par :
🏭 Une nouvelle usine (Bio 5)
Un nouveau site industriel majeur pour augmenter la capacité de production de vaccins pour chiens et chats. 55M de doses de vaccin seront produites par an, contre 35M de doses produites actuellement.
🔨 Une nouvelle ligne de remplissage de pointe
- Déploiement d’une nouvelle ligne de conditionnement aseptique de haute technologie : 9 millions d’euros d’investissement.
- Performance : jusqu'à 21 000 flacons de vaccins liquides par heure.
- Saut technologique : réduction du risque de contamination et respect des normes internationales les plus strictes
En se dotant de ces outils industriels modernes et compétitifs, nous cherchons à :
Sécuriser l'approvisionnement mondial des vétérinaires en vaccins
Répondre à la demande croissante en prévention portée par les vétérinaires.

Développer les technologies de l'industrie du futur.
La Bio Academy : l'expertise au service des compétences
Pour accompagner notre essor industriel, nous avons créé la Bio Academy à Carros, notre centre de formation interne. Cette académie répond à un double enjeu :
Soutenir l'investissement industriel :
- Maintenir et développer l'emploi local
- Maintenir l'excellence
- Monter en compétence : profils technologique et réglementaire
Intégrer et développer des compétences :
- Maitrise technique : création de Bio 5
- Ingénieur industrielle
- Plateforme technologiques de biologie
- Maitrise de la stérilité
L'objectif : consolider notre savoir-faire en biotechnologies pharmaceutiques sur le territoire français, un savoir-faire rare et très technique.
2. Des valences essentielles virales : 100% vivantes12
![raison-2-valences.png]()
-
Nos vaccins de routine utilisent des valences virales 100% vivantes. Ces vaccins vivants présentent de nombreux avantages comparés aux vaccins inactivés1 :

Immunité complète1,2,3
Ils déclenchent une immunité à la fois humorale et cellulaire, contrairement aux vaccins inactivés dont l'immunité est majoritairement humorale.

Protection rapide et durable1,2,3
L'apparition de la protection est plus rapide et sa durée généralement plus longue.

Proche de l'infection naturelle
Le virus se multiplie dans l'hôte sur les sites préférentiels de l'infection, simulant une réaction immunitaire naturelle pour une protection optimale.
3. Trois ans d'immunité
![picto-immunite-3ans.png]()
-
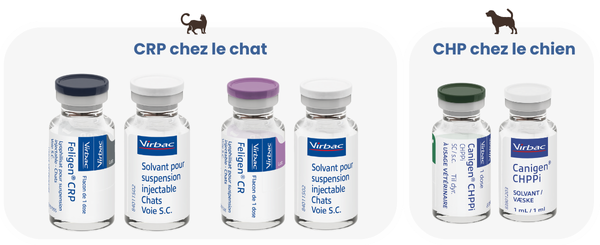
Grâce à la durée d'immunité démontrée de 3 ans, l'intervalle de vaccination peut être prolongé en fonction du risque d'exposition après le premier rappel annuel. Cette protection longue durée concerne plusieurs valences clés :
- Chez le chat : Valence leucose (Leucofeligen® FeLV/RCP, Leucogen®).
- Chez le chien : Maladie de Carré, Hépatite de Rubarth et Parvovirose (Canigen® CHPPi).
- Espèces communes : Rage (Rabigen® Mono).
4. Fraction de prévention
![raison-4-efficacite.png]()
-
Nos vaccins contenant la valence leucose démontrent un effet protecteur élevé avec une fraction de prévention de 86% à 3 ans sur la valence leucose8.
- Une étude randomisée et contrôlée sur 28 chats SPF* âgés de 9-10 semaines a été menée pour démontrer l'efficacité de Leucofeligen® FeLV/RCP 3 ans après l'injection de rappel annuel. 17 chats ont été vaccinés avec Leucofeligen® FelV/RCP vs 11 chats témoins8.
- Résultat sur la virémie : Les résultats montrent une fraction de prévention de 86 % contre la virémie persistante, 3 ans après la dernière injection8.
*Specific Pathogen Free (chat exempt d’organismes pathogènes spécifiques)
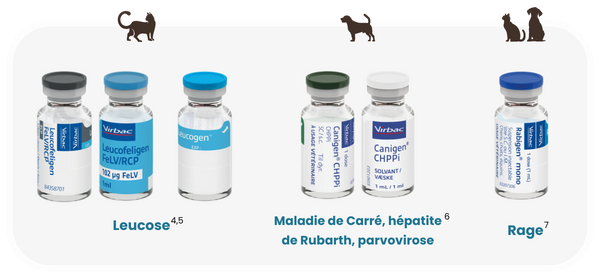
5. Début d'immunité précoce
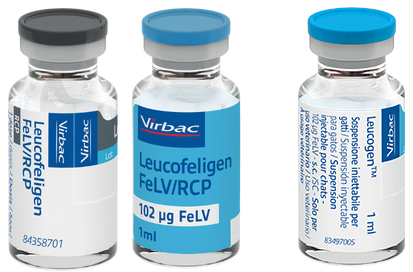
Début d’immunité précoce avec Leucofeligen® FeLV/RCP et Leucogen® 4,5
Valence calicivirus : début de l’immunité 3 semaines après la première injection de primovaccination (avec Leucofeligen® FeLV/RCP)
Valence leucose9 : la protection virale est observée chez 73 % des chats 3 semaines après la première injection du vaccin*
*étude réalisée sur le vaccin Leucogen sur 25 chatons âgés de 9 semaines en France en 2018
Vaccination précoce avec Canigen® CHPPi6
A partir de l’âge de 6 semaines
(suivie du schéma de vaccination habituel, à savoir : 2 injections à 3-4 semaines d’intervalle à 8 semaines d’âge)
6. FCV-F9 : une souche adaptée à la réalité du terrain en Europe
![raison-6-fcv-f9.png]()
-
La souche Calicivirus F9, utilisée depuis 20 ans adaptée à la réalité terrain en Europe10,11, offre une protection en phase avec les souches circulant actuellement.
97% de neutralisation croisée11
La capacité de neutralisation croisée large de la souche vaccinale FCV-F9 contre les souches terrains qui circulent actuellement en Europe a été confirmé in vitro.
![feligen-crp-r.png]()
-
- Etude d’envergure : 1521 échantillons pris au hasard provenant de 6 pays européens.
- Souches terrains de FCV : le FCV a été détecté dans 140 échantillons (9,2%) parmi lesquels 110 souches différentes de FCV.
- Large neutralisation croisée : les anticorps sériques induits par la vaccination contre le FCV-F9 ont neutralisé jusqu’à 97% des souches terrains testées.
- Résultats représentatifs : L’étendue et la randomisation de l’échantillonnage permettent d’établir que les isolats FCV étudiés sont largement représentatifs des FCV auxquels les chats sont exposés dans ces pays.
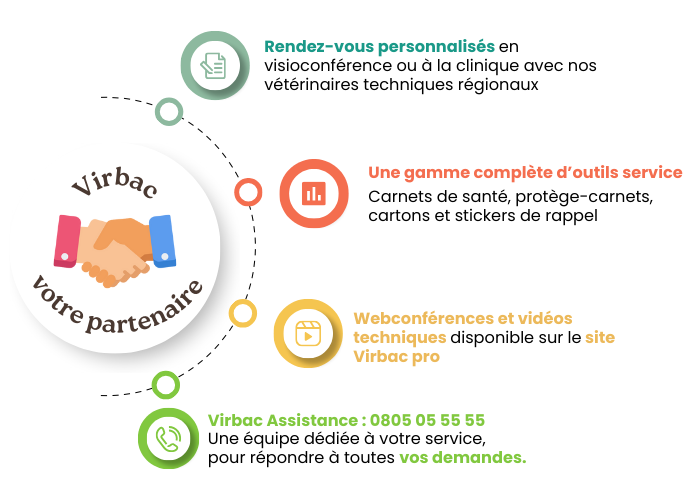
Une offre de service adaptée à vos besoins
Références :
1. Greene Book, Infectious Diseases of the dog and cat, 3rd edition, Greene CE et al, Saunders, Elsevier 2006
2.The 2006 American Associtation of Feline Vaccines Advisory Panel Report, Richards J, Hartmann K, Lappin M, Levy J et al, JAVMA, Vol 229, No.9, November 1, 2006
3. DiGangi B, Levy J, et al. (2011). Effect of maternally-derived antibodies on serologic responses to vaccination in kittens, Journal of Feline Medicine and Surgery 14(2) 118-123
4. RCP de Leucogen
5. RCP de Leucofeligen FeLV/RCP
6. RCP de Canigen CHPPi
7. RCP de Rabigen Mono
8. Données issues du dossier d’AMM de Leucogen et Leucofeligen FeLV/RCP.
9. Arcidiaco S et al. Onset of protection of FeLV vaccine containing purified p45 FeLV-enveloppe antigen after one single injection of primary vaccination in cats. 2023,Vaccines & Vaccination Vol 8, 2. Etude réalisée sur le vaccin Leucogen sur 25 chatons âgés de 9 semaines en France en 2018
10. Hou et al. (2016). European molecular epidemiology and strain diversity of feline calicivirus, Veterinary Record ; 178(5) : 114-5. Etude réalisée en France, Allemagne, Grèce, Portugal et Angleterre sur 426 chats (écouvillons oropharyngés) entre 2014 et 2015
11. Afonso et al. (2017). A multi-national European cross-sectional study of feline calicivirus epidemiology diversity and vaccine cross-reactivity, Vaccine ; 35(20):2753-2760. Étude réalisée en France, Italie, Allemagne, UK, Suède et Pays Bas sur 1521 chats (écouvillonsoropharyngés) entre 2013 et 2014.
12. Squires R.A et al. 2024 guidelines for the vaccination of dogs and cats-compiled by the Vaccination Guidelines Group (VGG) of the World Small Animal Veterinary Association (WSAVA). Journal of Small Animal Practice,2024, 1-40.
Numéro d'autorisation : AP 2026/4909
Mentions obligatoires
CANIGEN® CHPPI : Lyophilisat et solvant pour suspension injectable pour chiens. Composition : Une fois reconstituée, chaque dose de 1 mL contient : Substances actives : Lyophilisat : Virus de la maladie de Carré (CDV) souche Lederle vivant atténué 103 - 104,9 DICC50*, Adénovirus canin de type 2 (CAV-2) souche Manhattan vivant atténué 104 - 106 DICC50*, Parvovirus canin (CPV) souche CPV780916 vivant atténué 105-106,8 DICC50*, Virus parainfluenza canin (CPi V) souche Manhattan vivant atténué 105-106,9 DICC50*, (*) DICC50 : Dose infectant 50 % d’une culture cellulaire. Solvant : Eau pour préparations injectables. Espèce cible : Chiens. Indications : Chez les chiens, immunisation active en vue de : prévenir la mortalité et les signes cliniques causés par le CDV, prévenir la mortalité et les signes cliniques causés par l'adénovirus canin de type 1 (CAV-1), prévenir la mortalité et les signes cliniques et réduire l'excrétion causés par le CPV (étude d'efficacité réalisée avec la souche CPV-2b), prévenir les signes cliniques et réduire l’excrétion causés par le CPV (étude d’efficacité réalisée avec la souche CPV-2c), réduire les signes cliniques respiratoires et l’excrétion virale causés par le CPiV et CAV-2. Mise en place de l'immunité : à partir de 3 semaines après la primo-vaccination pour CDV, CAV-2 et CPV et à partir de 4 semaines pour CAV-1 et CPiV. Durée de l'immunité : Après la primovaccination : un an. Dans ces études portant sur la durée de l'immunité, il n'a pas été mis en évidence, 1 an après le schéma vaccinal, de différence significative entre le groupe vacciné et le groupe témoin en ce qui concerne l'excrétion virale de CPiV ou CAV-2. Après le premier rappel annuel, la durée d’immunité est de 3 ans pour CDV, CAV-1, CAV-2 et CPV et 1 an pour le CPiV. Pour CAV-2, la durée d’immunité après le premier rappel annuel n’a pas été établie par épreuve virulente et est basée sur la présence d’anticorps anti-CAV-2, 3 ans après le rappel de vaccination. Contre-indications : Aucune. Effets indésirables : Chiens : Fréquent (1 à 10 animaux / 100 animaux traités) : Gonflements au site d’injection1,2,3, œdème au site d’injection2,3,4, Léthargie2. Rare (1 à 10 animaux / 10 000 animaux traités) : Douleur au site d’injection2,3, prurit au site d’injection2,3,Hyperthermie2, anorexie2. Troubles du système digestif2 (par ex. diarrhée2, vomissements2). Très rare (< 1 animal / 10 000 animaux traités, y compris les cas isolés) :Réaction d’hypersensibilité (par ex. anaphylaxie, réaction allergique cutanée telle qu’œdème allergique, érythème urticarien, prurit allergique)5. 1 (≤ 4 cm). Chez les chiots âgés de 6 semaines, un gonflement (≤ 2 cm) parfois associé à une douleur et parfois suivi de nodules (≤ 0,1 cm), qui disparaît spontanément en 2 semaines ; peut être très fréquemment observé (voir la section « Symptômes de surdosage »). 2 Transitoire. 3 Disparaît spontanément en 1 à 2 semaines. 4 Légèrement diffus. 5 Un traitement symptomatique approprié doit être administré sans délai. Catégorie : Médicament vétérinaire soumis à ordonnance.
FELIGEN® CR : Lyophilisat et solvant pour suspension injectable pour chats. Composition : Une dose de 1 mL contient : Substances actives : Calicivirus félin vivant atténué, souche F9 104,6 à 106,1 DICC50(*), Herpèsvirus félin vivant atténué souche F2 105 à 106,6 DICC50(*), (*)DICC50 : dose infectant 50% des cultures cellulaires - Solvant : Eau pour préparations injectables. Espèce cible : Chats. Indications : Immunisation active contre la rhinotrachéite virale du chat et la calicivirose féline. Contre-indications : Aucune. Effets indésirables : Chats : Très rare (< 1 animal / 10 000 animaux traités, y compris les cas isolés) : Hyperthermie1, apathie1 Douleur au point d'injection2,3, tuméfaction au point d'injection2, nodule au point d'injection2 Réaction d'hypersensibilité4 1Au cours des 24 heures qui suivent la vaccination. 2Dans les jours suivant la vaccination, disparaît spontanément en 4 semaines au maximum. 3A la palpation. 4Observées chez certains animaux, requièrent un traitement symptomatique approprié. Catégorie : Médicament vétérinaire soumis à ordonnance.
FELIGEN® CRP : Lyophilisat et suspension pour suspension injectable. Composition : Une dose de 1 mL contient : Substances actives : Lyophilisat : Calicivirus félin, souche F9, vivant atténué 104,6 à 106,1 DICC50 (*), Herpèsvirus félin, souche F2, vivant atténué 105 à 106,6 DICC50 (*), Parvovirus félin, souche LR 72, vivant atténué, 103,7 à 104,5 DICC50(*), (*) DICC50 : dose infectant 50% des cultures cellulaires. Suspension : Virus rabique, souche VP12, inactivé, min. 1 UI (**). (**) UI Unité Internationale, titre minimal conforme aux exigences de la Pharmacopée Européenne. Adjuvant : Gel d’hydroxyde d’aluminium 3 % 0,10 mL. Espèce cible : Chats. Indications : Immunisation active contre la rhinotrachéite virale du chat, la calicivirose féline, la panleucopénie infectieuse féline et la rage. Des anticorps antirabiques sont détectés pendant 3 ans après le rappel de la valence rage. Contre-indications : Aucune. Effets indésirables : Chats : Très fréquent (> 1 animal / 10 animaux traités) : Désordres gastro-intestinaux1. Fréquent (1 à 10 animaux / 100 animaux traités) : Œdème au site d’injection1,2,3, Nodule au site d’injection1,2,3, Hyperthermie1,2,4, Léthargie1,4. Très rare (< 1 animal / 10 000 animaux traités, y compris les cas isolés) : Réaction d’hypersensibilité5 (Vomissement, Diarrhée, Dyspnée, Œdème allergique) Syndrome de boiterie fébrile6. 1 Transitoire(s). 2 Léger(ère). 3 Apparaissant durant les jours suivant la vaccination et disparaissant spontanément en 2 jours (œdème) ou 2 semaines (nodule, ≤ 2 mm). 4 De résolution spontanée. 5 En cas de réaction allergique ou anaphylactique, un traitement symptomatique approprié doit être administré. 6 Comme rapporté dans la littérature, chez les chatons après administration d’un vaccin contenant le Feline Calicivirus. Catégorie : Médicament vétérinaire soumis à ordonnance.
LEUCOFELIGEN® FeLV/RCP : Lyophilisat et suspension pour suspension injectable pour chats. Composition : Par dose de 1 ml : Lyophilisat : Substances actives : Calicivirus félin vivant atténué (souche F9) 104,6 - 106,1 DICC50*, Virus vivant atténué de la Rhinotrachéite Virale féline (souche F2) 105,0 - 106,6 DICC 50*, Virus vivant atténué de la Panleucopénie féline (souche LR 72) 103,7 - 104,5 DICC50*, (*DICC 50 : *dose infectant 50% d’une culture cellulaire). Excipients : Tampon stabilisant contenant de la gélatine QSP 1,3 ml avant lyophilisation. Suspension : substance active : quantité minimale d’antigène purifié p45 de l’enveloppe du FeLV 102 µg, Adjuvants : Gel d’hydroxyde d’aluminium à 3% exprimé en mg d’Al3+ 1 mg, Extrait purifié de Quillaja saponaria 10 µg. Excipient : Solution isotonique tamponnée QSP 1 ml. Espèce cible : Chats. Indications : Pour l’immunisation active des chats à partir de l’âge de 8 semaines contre : la calicivirose féline pour réduire les signes cliniques, la rhinotrachéite virale féline pour réduire les signes cliniques et l'excrétion virale, la panleucopénie féline pour prévenir la leucopénie et réduire les signes cliniques, la leucose féline pour prévenir la virémie persistante et les signes cliniques de la maladie associée. Le début de l'immunité a été démontrée à partir de : - 3 semaines après la première injection de la primovaccination pour la valence calicivirus, - 3 semaines après la primovaccination pour les valences panleucopénie et leucose, - 4 semaines après la primovaccination pour la valence du virus de la rhinotrachéite. Après la primovaccination, la durée de l'immunité est de un an pour tous les composants. Après le premier rappel de vaccination un an après la primovaccination, une durée d'immunité de 3 ans a été démontrée pour la valence leucose. Contre-indications : Aucune. Effets indésirables : Après la première injection, une réaction locale transitoire et modérée (≤ 2 cm) est communément observée. Cette réaction locale peut être une tuméfaction, un œdème ou un nodule et régresse spontanément en 3 à 4 semaines au maximum. Cette réaction est nettement plus légère après la deuxième injection et les administrations suivantes. Suite à la vaccination, des signes transitoires tels qu’une hyperthermie (durant 1 à 4 jours), une apathie ou des troubles digestifs, peuvent également être fréquemment observés. Dans de rares cas, l’animal peut présenter une douleur à la palpation, des éternuements ou une conjonctivite, qui disparaissent sans traitement. Dans de très rares cas, des réactions anaphylactiques ont été signalées. En cas de choc anaphylactique, un traitement symptomatique approprié doit être administré. Comme rapporté dans la littérature, l'utilisation d'un vaccin contenant le Feline Calicivirus peut entraîner dans de très rares cas une réaction de syndrome de boiterie fébrile chez les chatons. Catégorie : Usage vétérinaire. Vaccin : délivrance soumise à ordonnance.
LEUCOGEN® : Suspension injectable pour chats. Composition : Par dose de 1 ml : Substance active : Quantité minimale d’antigène purifié p45 de l’enveloppe du FeLV : 102 µg. Adjuvants : gel d’hydroxyde d’aluminium à 3% exprimé en mg d’Al3+ 1 mg, extrait purifié de Quillaja saponaria 10 µg. Espèce cible : Chats. Indications : Pour l’immunisation active des chats à partir de l’âge de 8 semaines contre la leucose féline pour prévenir la virémie persistante et les signes cliniques de la maladie associée. Début de l'immunité : 3 semaines après la primovaccination. Durée de l'immunité : Après la primovaccination, la durée de l'immunité dure un an. Après le premier rappel de vaccination un an après la primovaccination, une durée d'immunité de 3 ans a été démontrée. Contre-indications : Aucune. Effets indésirables : Fréquent (1 à 10 animaux / 100 animaux traités) : Réaction au site d’injection1 , Tuméfaction au site d’injection1 , Œdème au site d’injection1 , Nodule au site d’injection1 Hyperthermie2,3, Apathie3 Troubles digestifs3. Rare (1 à 10 animaux / 10 000 animaux traités) : Douleur au site d’injection4,5 Éternuement5 Conjonctivite5. Très rare (<1 animal / 10 000 animaux traités, y compris les cas isolés) : Anaphylaxie (réaction allergique sévère)6. 1 Une réaction locale transitoire et modérée (≤2 cm) est observée après la première injection ; elle disparaît spontanément en 3 à 4 semaines au maximum. Cette réaction est nettement plus légère après la seconde injection et les administrations suivantes. 2 Durant 1 à 4 jours. 3 Signes transitoires. 4 À la palpation. 5 Disparaît sans traitement. 6 En cas de choc anaphylactique, un traitement symptomatique approprié doit être administré. Catégorie : Médicament vétérinaire soumis à ordonnance.
RABIGEN® MONO : Suspension injectable pour chiens, chats et équins. Composition : Une dose de 1 mL contient : Substance active : Virus rabique inactivé, souche VP12 ... ≥1 Unité Internationale (*). Gel d'hydroxyde d'aluminium 3 % ... 0,10 mL. (*) Titres minimaux conformes aux exigences de la Pharmacopée Européenne. Espèces cibles : Chats, chiens, équins. Indications : Immunisation active contre la rage. Durée de l’immunité : Chez les chiens : 3 ans après le premier rappel. Chez les chats : des anticorps antirabiques sont détectés pendant 3 ans après le premier rappel. Contre-indications : Aucune. Effets indésirables : Chiens, chats et équins : Très rare (< 1 animal / 10 000 animaux traités, y compris les cas isolés) : Vomissements1. Fréquence indéterminée (ne peut être estimée à partir des données disponibles) : Œdème au site d’injection1,2, Tuméfaction au site d’injection1,2, Réactions d’hypersensibilité. 1 Chez les chiens et les chats. 2Légers, apparaissant durant les heures qui suivent l’administration, parfois douloureux à la palpation et disparaissant spontanément en quelques heures sans traitement particulier. Catégorie : Médicament vétérinaire soumis à ordonnance.






.png)
.png)